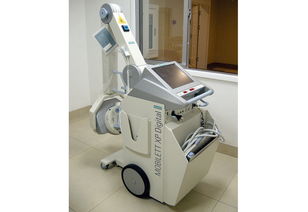
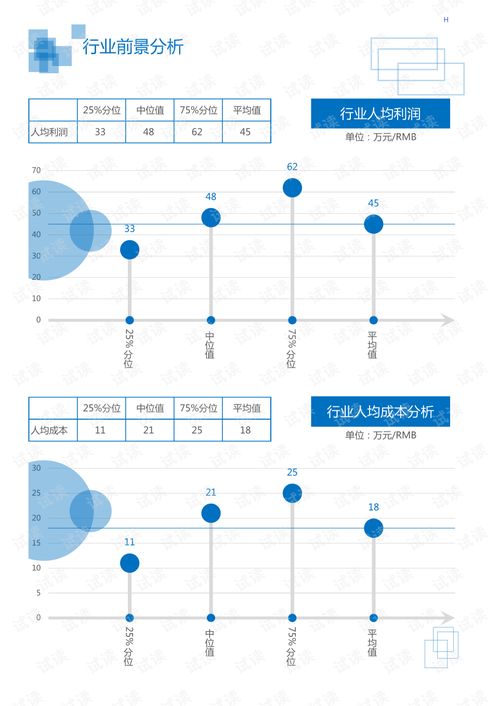
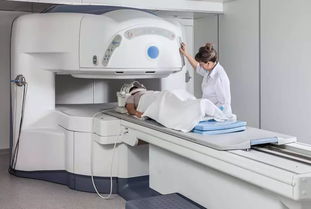
随着我国医疗器械监管体系的不断完善,进口医疗器械注册管理也迎来了新的调整。需要注意的是,通信设备本身并不属于医疗器械范畴,但部分医疗器械(如远程医疗设备、可穿戴健康监测设备等)可能集成通信功能。因此,针对这类兼具医疗器械和通信特性的产品,注册时需同时满足医疗器械监管和通信设备相关的法规要求。
一、医疗器械注册核心要求
- 分类管理:根据风险等级,医疗器械分为I、II、III类,需按照相应类别提交注册申请。
- 技术文件:需提供产品技术要求、检测报告、临床评价资料(如适用)、风险管理文件等。
- 质量管理体系:境外生产企业需通过我国药品监督管理部门认可的质量管理体系核查。
- 标签说明书:中文标识,内容符合《医疗器械说明书和标签管理规定》。
二、集成通信功能的特殊要求
- 电磁兼容性:需符合YY 0505(医用电气设备电磁兼容性要求)及相关国家标准,确保通信功能不影响医疗器械的安全有效。
- 数据安全:若涉及患者数据无线传输,需满足《医疗器械网络安全注册审查指导原则》,确保数据完整性、保密性。
- 通信标准:使用的通信模块(如蓝牙、Wi-Fi、4G/5G)需获得我国进网许可,符合《电信设备进网管理办法》。
三、注册流程优化
新规推行电子申报,审评时限进一步明确。对于创新医疗器械,可申请优先审评,加速上市进程。
四、企业应对建议
- 提前规划:结合产品特性,明确医疗器械主类别和通信相关附加要求。
- 合规测试:在国内外实验室完成医疗器械安全性和通信模块入网检测。
- 本地支持:建议与境内代理人紧密合作,高效应对监管问询。
综上,进口医疗器械若集成通信功能,企业需统筹医疗器械注册和通信设备合规双重要求,提前布局,以确保产品顺利进入中国市场。